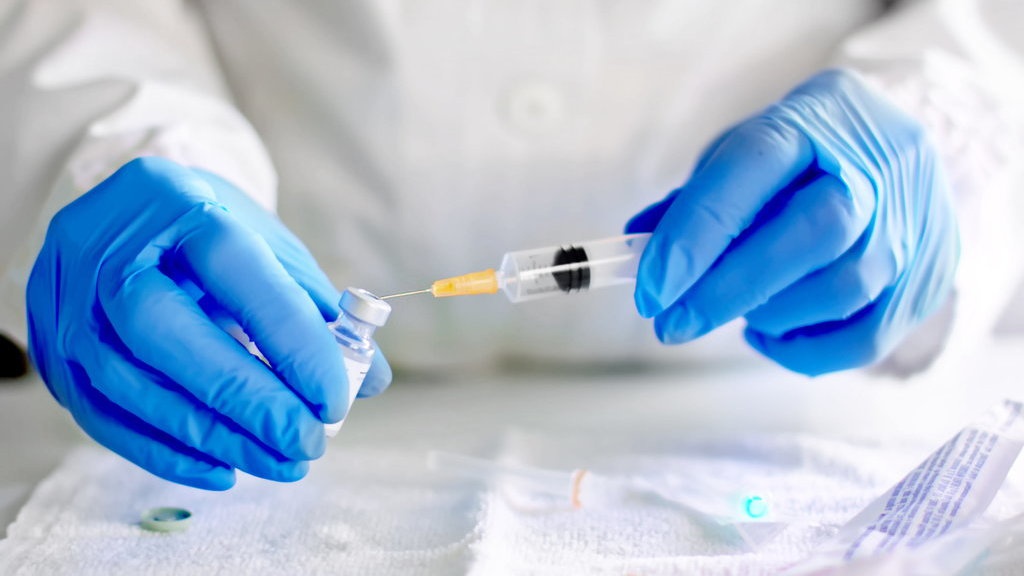
tirto.id - Juru Bicara Satgas Penanganan Covid-19 Wiku Adisasmito meyakinkan bahwa vaksin Covid-19 yang saat ini sedang tahap uji klinis fase 3 aman digunakan manusia. Sebab, vaksin adalah virus yang dilemahkan dan pada prinsipnya vaksin tidak berbahaya.
Menurut Wiku vaksin yang masuk ke tubuh manusia akan menstimulasi imunitas tubuh. Vaksin Covid-19 tidak saja akan melindungi diri sendiri, juga orang lain yang tidak mendapatkan vaksinasi karena alasan tertentu, termasuk alasan kesehatan.
"Pemerintah memastikan vaksin Covid-19 aman untuk digunakan manusia, karena harus melalui tahapan uji praklinis dan klinis untuk memastikan keamanan, efektifitas dan dosis yang aman untuk digunakan manusia. Risiko yang ditimbulkan vaksin sangat rendah dan manfaat jauh lebih tinggi," jelasnya menjawab pertanyaan media dalam konferensi pers virtual, Selasa (10/11/2020).
Masih menjawab pertanyaan media terkait vaksin, Satgas Penaganan Covid-19 menegaskan bahwa pembangunan laboratorium milik TNI di Pulau Galang, saat ini masih dalam tahap perencanaan.
"Laboratorium yang akan dibangun ditujukan untuk penelitian virus yang akan dikembangkan menjadi vaksin," jawab Wiku.
Prosedur Pengadaan Vaksin Covid-19 di Indonesia
Pada akhir Oktober lalu, Ketua Tim Penanganan Covid-19 dan Pemulihan Ekonomi Nasional (PC-PEN), Menko Perekonomian Airlangga Hartarto mengatakan jutaan dosis vaksin Covid-19 akan masuk ke Indonesia pada bulan Desember 2020.
"Dari Sinovac, akan ada dalam bentuk [vaksin] jadi, sekitar 3 juta [dosis]. Dan, itu akan masuk ke Indonesia secara bertahap," kata Airlangga, dalam talskhow yang disiarkan akun Youtube BNPB.
Selain mengirim vaksin dalam bentuk jadi, kata Airlangga, Sinovac juga akan mengirimkan bahan baku kepada Bio Farma (BUMN). Jumlah bahan baku vaksin Covid-19 kiriman dari Sinovac tersebut setara dengan 15 juta dosis.
Sinovac merupakan perusahaan farmasi asal Tiongkok. Perusahaan itu kini sedang menuntaskan proses uji klinis tahap 3 vaksin Covid-19 di beberapa negara, termasuk Indonesia. Di tanah air, perusahaan ini menggandeng Bio Farma untuk pelaksaan uji klinis tahap III vaksin Covid-19.
Airlangga menegaskan, pengadaan vaksin dari Sinovac tetap harus melalui proses verifikasi dari Badan Pengawas Obat dan Makanan (BPOM) RI. Setelah ada izin BPOM, vaksin Sinovac baru dapat digunakan di Indonesia.
"Vaksin, pintunya di BPOM. [....] Kuncinya ada di BPOM," ujar Airlangga.
Untuk mendapat izin berupa emergency use authorization (UEA) dari BPOM, vaksin buatan Sinovac harus memenuhi sejumlah persyaratan terkait keamanan penggunaannya, serta memenuhi semua prosedur uji klinis.
BPOM akan melakukan evaluasi dan menganalisis laporan hasil uji klinis vaksin Sinovac, termasuk dari negara-negara lain. Kata Airlangga, BPOM sudah mengirimkan tim yang melihat proses pembuatan vaksin di Tiongkok, dan sejumlah negara lain, termasuk Inggris.
"Jika seluruh syarat terpenuhi [ada izin dari BPOM], baru dilakukan imunisasi dengan perencanaan matang," ia menambahkan. "Ini akan bisa dimulai, setelah BPOM sudah mengeluarkan emergency use authorization."
Kehadiran vaksin menjadi harapan utama untuk meredam pandemi Covid-19. Selama ini, vaksin terbukti efektif mencegah infeksi beragam penyakit.
Salah satu kesuksesan vaksin adalah musnahnya penyakit smallpox (cacar). Dahulu, 1 dari 3 orang yang menderita smallpox, meninggal. Campak dan polio juga bisa diatasi dengan adanya vaksin.
Namun, pembuatan vaksin tidak mudah. Dimulai dari pembuatan bibit vaksin, ia dikembangkan dalam satu rangkaian pengujian ke hewan dan manusia.
Pengujian vaksin ke manusia dilakukan melalui uji klinis tahap I, II, dan III. Rangkaian pengujian itu untuk memastikan bahwa vaksin aman dan tidak berdampak negatif pada kesehatan manusia, sekaligus efektif mencegah infeksi.
------------------------------------------
Artikel ini terbit atas kerja sama Tirto.id dengan Badan Penanggulangan Bencana Nasional (BNPB).
Editor: Agung DH
 Masuk tirto.id
Masuk tirto.id