tirto.id - Belum lama ini pengadilan arbitrase internasional PBB, United Nations Commission International Trade Law (UNCITRAL) menolak gugatan Eli Lilly. Perusahaan farmasi Amerika Serikat ini pun kalah terhadap sengketa dengan pemerintah Kanada. Gugatan dengan nilai kompensasi 500 juta dolar Kanada bermula saat pengadilan federal Kanada membatalkan paten atas bahan baku obat atomoxetine dan olanzapine. Merek obat Eli Lilly, Strattera dan Zyprexa yang bahan bakunya mengandung atomoxetine dan olanzapine dianggap tidak memberikan kegunaan lebih.
Kanada bahkan menilai obat produksi Eli Lilly tidak memenuhi standar paten karena percobaan klinisnya hanya melibatkan 22 pasien. Terlalu kecil untuk membuktikan bahwa Strattera dan Zyprexa lebih baik dari obat yang ada di pasaran Kanada. Paten atas strattera (atomoxetine) didaftarkan LLY pada 4 Januari 1996 dan seharusnya berakhir pada tahun 2016. Pengadilan Federal Kanada membatalkan paten atas Atomoxetine di tahun 2010.
Sementara, paten atas Olanzapine (Zyprexa) didaftarkan pada 24 April 1991 dan dibatalkan pada 10 November 2011. “LLY menganggap pembatalan paten Kanada ini merugikan bisnis mereka. Jadi mereka gugat Kanada,” ujar peneliti Indonesia for Global Justice (IGJ) Lutfiyah Hanim dalam sebuah diskusi di Jakarta (7/2/2017).
Untuk mengawasi peredaran obat paten, Kanada telah memiliki standar domestik bagi para produsen farmasi yang memiliki obat paten. Saat pendaftaran, perusahaan farmasi harus mampu membuktikan obat yang dipatenkannya lebih bagus dibandingkan obat yang sudah ada di pasaran. Pemberian paten merupakan insentif penelitian dan pengembangan produk dengan jaminan kembalinya dana investasi melalui penjualan produk komersial.
Kontroversi yang sering terjadi adalah harga obat baru menjadi sangat mahal dan tidak terjangkau. Kasus Eli Lilly versus Kanada bisa dialami oleh negara-negara lainnya. Apalagi negara-negara pemilik paten obat seperti Amerika Serikat selalu berupaya untuk mengamankan hak paten obat dan berlindung di bawah perjanjian perdagangan Internasional—termasuk North American Free Trade Agreement (NAFTA) di dalamnya ada klausul investor-state dispute settlement (ISDS) yang jadi dasar Eli Lilly menggugat Kanada.
Skema perjanjian perdagangan multinasional salah satunya bertujuan untuk memelihara monopoli obat oleh produsen farmasi. Dampaknya, akses masyarakat negara berkembang terhadap obat makin tak terjangkau. Di sektor akses obat-obatan jelas hal ini akan mengancam Indonesia yang sekitar 70 persen rakyatnya menggunakan obat generik.
“Ini mengerikan, jika kita mau menyediakan akses obat murah dan berkualitas tapi dihadapkan masalah paten yang dimiliki perusahaan obat besar,” kata Sindi Putri, Advocacy Officer Indonesia AIDS Coalition (IAC) kepada Tirto.
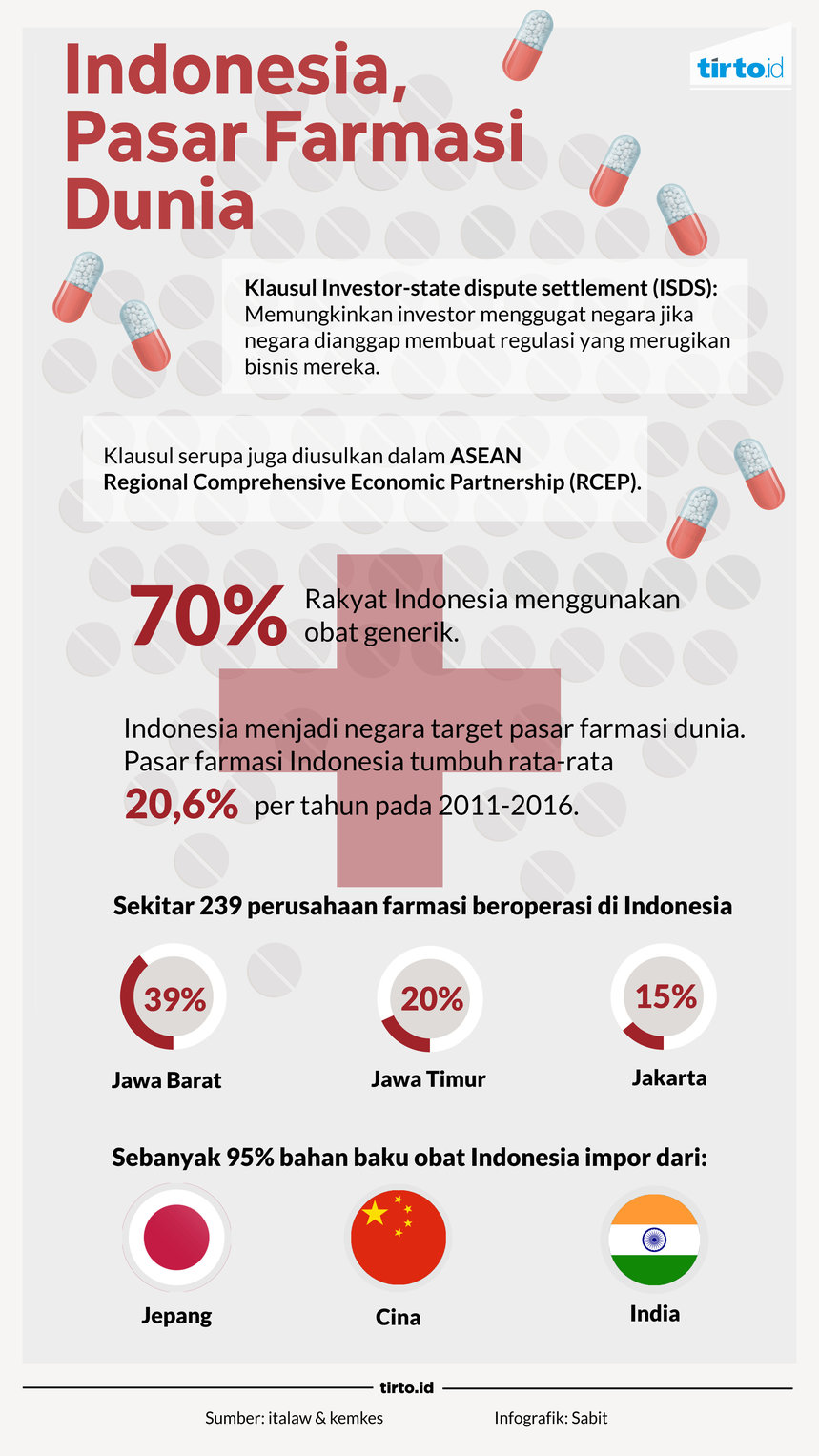
Skema semacam ISDS rencananya akan masuk dalam perjanjian ASEAN Regional Comprehensive Economic Partnership (RCEP) yang masih tahap negosiasi. RCEP sebuah kerjasama ekonomi dan perdagangan di kawasan ASEAN dengan enam negara mitra lainnya, yakni: China, Jepang, Korea Selatan, India, Australia, dan New Zealand. Selain itu, dalam perjanjian World Trade Organization (WTO) secara tegas ada klausul Trade Related Aspects of Intellectual Property Rights (TRIPs).
TRIPs mensyaratkan adanya perlindungan paten secara universal untuk setiap penemuan di bidang teknologi termasuk di bidang farmasi. Namun, terdapat tiga celah fleksibilitas dalam TRIPs yang dapat digunakan setiap negara anggota WTO untuk melindungi kesehatan rakyatnya, yakni impor paralel, lisensi wajib dan penggunaan oleh pemerintah. Negara-negara kuat dalam industri farmasi seperti Amerika Serikat serta Uni Eropa justru mendorong adanya ketentuan perlindungan atas hak kekayaan intelektual yang lebih tinggi dari TRIPs, yakni TRIPs plus.
“Perjanjian TRIPS fleksibilitas yang diatur WTO agar beragam jenis obat dapat diakses saat mendesak, menjadi jadi tidak berlaku. Sementara kita sangat mendorong TRIPs fleksibilitas diimplementasikan di negara kita agar memudahkan akses obat,” kata Sindi.
Indonesia termasuk negara yang sudah meratifikasi aturan main WTO yang secara tegas diakui dalam Undang-undang No.7/1994 tentang Persetujuan Pembentukan Organisasi Perdagangan Dunia. Secara detil terkait obat paten Dalam UU No. 14 Tahun 2001 tentang paten, yang kemudian direvisi menjadi UU No 13 Tahun 2016 mengatur masa berlaku paten di Indonesia diterapkan selama 20 tahun.
Pada jangka tahun tersebut, pemegang paten seperti perusahaan farmasi memiliki hak eksklusif untuk melarang pihak lain yang tanpa persetujuannya untuk membuat, menggunakan, menjual, mengimpor, menyewakan, menyerahkan, atau menyediakan untuk dijual atau disewakan atau diserahkan produk yang diberi paten. Keistimewaan ini sering dikonotasikan dengan monopoli obat, terutama dampaknya pada harga di konsumen yang terlalu tinggi.
Komisi Pengawas Persaingan Usaha (KPPU) sempat menyoroti soal harga obat paten. Wasit persaingan usaha ini sejak beberapa tahun lalu mewanti-wanti tidak adanya regulasi yang mengatur harga eceran tertinggi (HET) untuk obat paten yang diproduksi oleh perusahaan farmasi asing. Dampaknya harga obat paten dan obat generik sangat terpaut jauh sehingga harus diatur soal harganya.
"Klasifikasi obat mulai dari obat paten, obat branded, dan obat generik, ke depan bisa kita dorong supaya harganya agar tidak terlalu timpang," kata Ketua KPPU Syarkawi Rauf dikutip dari Antara, Februari 2017.
Obat paten memang pengakuan terhadap hak intelektual terhadap penemuan terbaru. Namun, pengawasan terhadap keberadaaan obat paten harus dilakukan dari proses pendaftaran, pengakuan, penetapan harga obat paten. Jangan sampai obat paten jadi perangkap monopoli yang tak terkendali.
Penulis: Aditya Widya Putri
Editor: Suhendra
 Masuk tirto.id
Masuk tirto.id






























