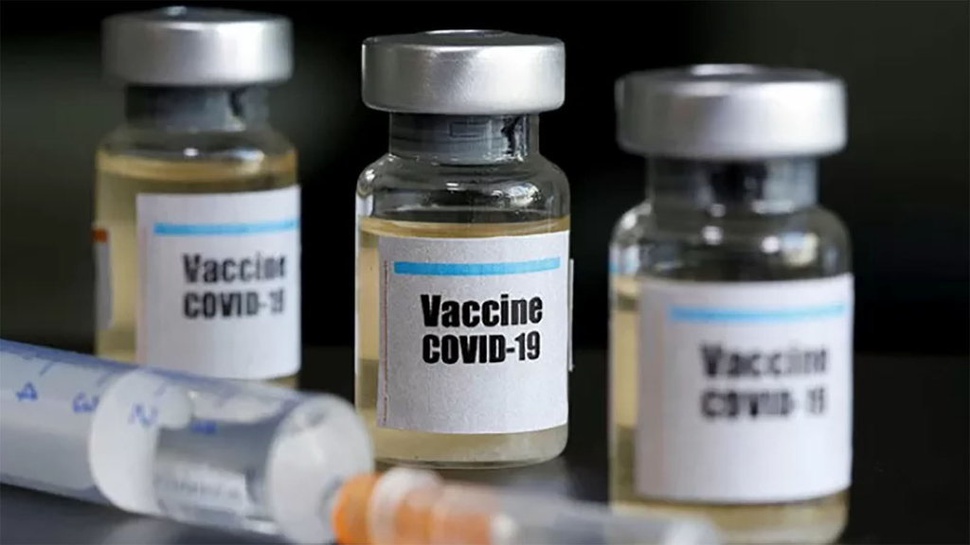
tirto.id - Direktur Registrasi Obat Badan Pengawas Obat dan Makanan (BPOM) Lucia Rizka Andalusia menyatakan dalam hal penyediaan vaksin COVID-19, pihaknya mengawal khasiat, keamanan dan mutu, mulai dari pelaksanaan uji klinik sebagai bagian dari pengembangan produk vaksin, proses produksi, hingga peredaran di masyarakat.
Sebagai bentuk pengawalan terhadap khasiat, keamanan dan mutu vaksin Corona, salah satu upaya jajarannya ialah dengan inspeksi cara pembuatan obat yang baik (CPOB).
“Hari ini tim Inspektur CPOB BPOM berangkat ke Tiongkok untuk menginspeksi CPOB di fasilitas produksi vaksin yang akan dibeli oleh pemerintah Indonesia,” ujar dia, Kamis (15/10/2020).
Inspeksi tersebut bertujuan agar BPOM memastikan mutu vaksin, pengamatan terhadap kepatuhan industri, dan memproduksi vaksin sesuai dengan persyaratan CPOB. Tim Inspektur yang berangkat bersama dengan Lembaga Pengkajian Pangan, Obat-obatan, dan Kosmetika Majelis Ulama Indonesia (LPPOM MUI), Kementerian Kesehatan dan PT Bio Farma akan melakukan inspeksi ketiga sarana produksi yang ada di Tiongkok yaitu Sinovac, Sinopharm, dan Cansino.
“Inspeksi tersebut ditujukan untuk mempercepat akses vaksin yang aman, berkhasiat, dan bermutu di Indonesia,” imbuh Lucia. Dari segi khasiat keamanan vaksin, BPOM mengawal uji klinik (penyusunan protokol, pemberian persetujuan pelaksanaan dan pelaksanaan). Pengawalan ini memberlakukan inspeksi berkala untuk melihat pemenuhan kaidah uji klinik.
Sejauh ini tak ada laporan efek samping serius dari pemberian vaksin dalam uji klinik. Kemudian, uji klinik vaksin COVID-19 yang dilakukan oleh tim peneliti dari Fakultas Kedokteran Universitas Padjajaran memasuki tahap akhir rekrutmen subjek penelitian. Diharapkan pada 16 Oktober, ada 1.620 subjek rampung direkrut lantaran uji klinik fase tiga ini berlangsung sejak 11 Agustus 2020.
Lucia melanjutkan, untuk menyiapkan fasilitas produksi vaksin di Indonesia, BPOM mengadakan rapat koordinasi persiapan industri farmasi perihal ketersediaan vaksin dan komitmen pemenuhan aspek khasiat, keamanan, dan mutu vaksin.
Selanjutnya, pada masa pandemi COVID-19 memungkinkan diberikannya emergency use authorization (EUA/otorisasi penggunaan darurat) sesuai dengan Peraturan BPOM Nomor 27 Tahun 2020 tentang Perubahan Kedua atas Peraturan Kepala BPOM Nomor 24 Tahun 2017 tentang Kriteria dan Tata Laksana Registrasi Obat. Izin penggunaan darurat tersebut diberikan karena semua vaksin dan obat yang akan digunakan dalam penanganan Corona masih dalam pengembangan.
Obat dan vaksin yang mendapat EUA harus didukung bukti keamanan, khasiat, dan mutu yang memadai, sehingga dapat digunakan meskipun harus tetap memantau khasiat dalam populasi yang lebih besar dan keamanan yang lebih ketat. BPOM pun juga berkesinambungan melakukan pengawasan, penyaluran, dan peredaran terhadap obat/vaksin impor; proses produksi di industri dalam negeri; distribusi oleh pedagang besar bidang farmasi; dan distribusi di sarana kefarmasian.
“BPOM sangat berhati-hati dalam percepatan ketersediaan obat dan kepastian untuk mendapatkan akses terhadap vaksin ini. Pengawasan juga dilakukan melalui evaluasi laporan efek samping obat, realisasi importasi obat, produksi dan distribusi obat yang disampaikan ke BPOM oleh industri farmasi.
Penulis: Adi Briantika
Editor: Restu Diantina Putri