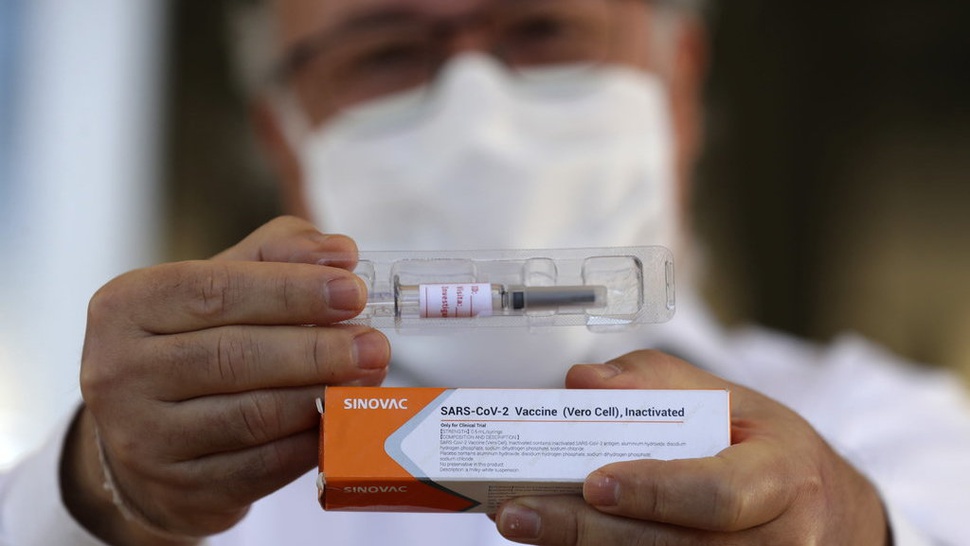
tirto.id - Badan Pengawas Obat dan Makanan (BPOM) menyebut hasil uji klinik tahap 3 vaksin Sinovac belum menemukan efek samping serius kepada pasien.
“Dari hasil inspeksi yang dilakukan, sejauh ini uji klinik telah dilaksanakan dengan baik. Belum ada KTD atau efek samping serius yang dialami oleh subjek uji klinik,” ungkap Kepala Badan POM Penny Lukito dalam keterangan, Kamis (19/11/2020).
BPOM pun akan memonitor penggunaan vaksin COVID-19. Hasil monitor atas relawan ini dilakukan juga oleh Komite Etik Penelitian Kesehatan Universitas Padjadjaran.
Penny menuturkan, BPOM terus memonitor proses uji vaksin Sinovac pada suntikan pertama dan suntikan kedua (14 hari setelah suntikan pertama) vaksin.
Uji coba vaksin tersebut sudah diberikan kepada 1.620 relawan. BPOM akan menerbitkan izin jika tidak ada kendala dalam proses pengamatan usai suntikan kedua.
“Untuk dapat diterbitkan persetujuan penggunaan atau izin edar, vaksin harus memenuhi persyaratan keamanan, khasiat, dan mutu sesuai standar yang telah ditetapkan. Data khasiat dan keamanan diperoleh dari hasil uji klinis, sementara data mutu diperoleh dari pemenuhan spesifikasi produk vaksin dari bahan awal hingga produk jadi,” kata Penny.
BPOM juga melakukan inspeksi ke fasilitas produksi Sinovac pada 2-5 November 2020 lalu untuk memastikan standar cara pembuatan obat seperti proses pembuatan bahan baku, formulasi vaksin hingga bentuk jadi.
Data tersebut lantas dikelola dan dievaluasi berdasarkan standar pedoman evaluasi nasional dan internasional. Proses evaluasi dilakukan oleh Badan POM melalui pembahasan bersama Komite Nasional Penilai Obat, tenaga ahli, dan klinisi dari Ikatan Dokter Indonesia. Khusus untuk vaksin, pembahasan dilakukan bersama ITAGI (Indonesia Technical Advisory Group on Immunization).
“Kami berharap agar PT Biofarma dan Sinovac Biotech China berkomitmen untuk memenuhi data-data tersebut, sehingga pemberian izin dapat segera dilakukan oleh Badan POM sesuai dengan rencana vaksinasi yang ditetapkan oleh Pemerintah,” tegas Penny.
Di saat yang sama, Penny mengatakan BPOM mempermudah izin edar vaksin COVID-19 dengan simplifikasi prosedur dan persyaratan, tanpa mengabaikan aspek keselamatan manusia dan kualitas vaksin. Dalam hal ini, izin dikeluarkan dalam bentuk perizinan penggunaan vaksin dalam kondisi darurat atau Emergency Use Authorization (EUA).
Syarat pemberian EUA adalah vaksin harus sudah memiliki data uji klinis fase 1 dan uji klinis fase 2 secara lengkap, serta data analisis interim uji klinis fase 3 untuk menunjukkan khasiat dan keamanan. Prosedur EUA ini mengacu pada pedoman persetujuan emergensi dari WHO (WHO Emergency Listing), US Food and Drug Administration (EUA), dan European Medicines Agency/EMA (Conditional Approval).
Setelah vaksin mendapat izin persetujuan penggunaan, BPOM akan mengawal mutu vaksin di sepanjang jalur distribusi nantinya akan menjadi tanggung jawab dari industri farmasi dan distributor yang ditunjuk.
BPOM juga melakukan pengawasan dan pendampingan dalam penerapan Cara Distribusi Obat yang Baik karena vaksin merupakan Produk Rantai Dingin (Cold Chain Product) yang sensitif terhadap perubahan suhu, sehingga upaya dan kontrol yang ketat di sepanjang jalur distribusi sangat diperlukan agar mutu dan stabilitas vaksin tetap terjaga sampai kemudian digunakan oleh end-user (pasien).
“Kami berharap semua pihak berkomitmen dan saling mendukung untuk bersama mengupayakan keberhasilan rencana pelaksanaan vaksinasi dalam rangka penanganan pandemi COVID-19 di Indonesia,” tutur Penny.
Penulis: Andrian Pratama Taher
Editor: Maya Saputri