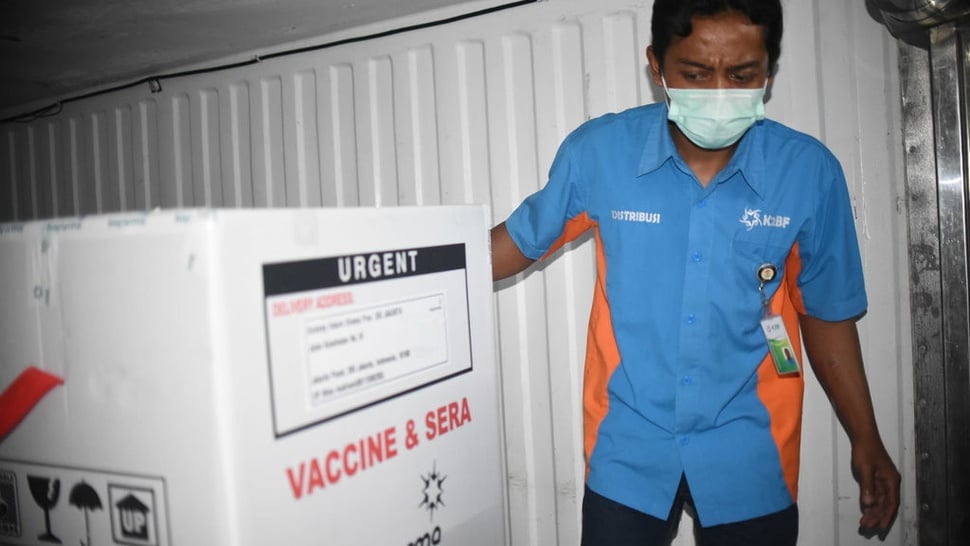
tirto.id - Kepala Badan Pengawas Obat dan Makanan (BPOM) Penny Lukito mengatakan izin penggunaan darurat atau emergency use authorization (EUA) vaksin Sinovac masih menunggu hasil uji klinis fase 3 yang dilakukan di Bandung, Jawa Barat.
“Kami masih menunggu hasil uji klinis fase 3 yang ada di Bandung untuk pengamatan interim tiga bulan yang akan diberikan hari ini. Jadi hari ini kami terima dan secepatnya kita bahas bersama dalam waktu tidak lama,” kata Penny dalam keterangan pers melalui daring, Jumat (8/1/2021).
Terkait hasil uji klinis di Bandung, kata dia, sudah masuk dalam tahap pembahasan akhir dan hari ini masih dalam pembahasan. Setelah itu data akan diberikan seluruhnya ke BPOM untuk dibahas dan dianalisa secara internal.
Setelah itu BPOM akan melakukan pembahasan akhir dengan para Komisi Nasional Penilaian Obat. Dalam pembahasan itu melibatkan Indonesian Technical Advisory Group on Immunization (ITAGI), klinisi dan para epidemiolog.
Selain menggunakan data hasil uji di Bandung, BPOM dalam mengeluarkan EUA juga menggunakan data hasil uji vaksin Sinovac yang ada di Brazil dan Turki. Sebelumnya, hasil uji klinik di Brazil telah memaparkan data uji mencapai 78 persen. Sementara di Turki, mencapai 91 persen.
Penny mengatakan, perbedaan hasil uji ini terjadi karena faktor jumlah subjek. Namun demikian hasil uji tersebut menurutnya sudah berada di atas standar WHO yakni di atas 50 persen.
Ia menjelaskan, BPOM akan menggunakan beberapa pedoman dalam penerbitan izin. Adapun pedoman tersebut di antaranya dari Badan Kesehatan Dunia (WHO) dan European Medical Agency.
"Untuk EUA vaksin harus memiliki data uji klinik fase satu dan dua secara lengkap dalam 6 bulan pemantauan serta data interim fase tiga untuk menunjukkan khasiat dan keamanan," ujarnya.
Pun demikian dengan vaksin lain yang telah mendapatkan UEA dari negara lain, jika hendak digunakan di Indonesia maka juga akan melalui izin dari BPOM. Namun untuk vaksin yang telah mendapatkan UEA dari negara-negara tertentu proses perizinan, kata Penny, akan lebih mudah.
Penulis: Irwan Syambudi
Editor: Abdul Aziz